



来源:药物临床试验机构办公室
时间:2025-04-03
浏览量:
分享:
一、研究室概况
同济医院I期临床试验研究室成立于2004年,2006年获批药物临床试验资格。
研究室建筑面积1385平方米,拥有大观察室3间,VIP观察室5间,病床60余张,可同时开展多个项目,能满足不同类型的临床研究需求。

研究室具有独立的受试者筛查区、知情同意室、受试者活动区、工作区、抢救室、配餐间、配药室、药品储藏间、样本处理室、样本储藏间、资料室、体格检查室、监控室、采血间等。


二、研究团队
主任:胡俊波
副主任:吕家高、徐沙贝、刘东
办公室主任:李娟
项目管理:任秀华
研究室配有专职医生1名,兼职医生约8名;专职护士3名,兼职护士约50名;质量控制(QA)2名;专职药学人员6名,兼职约10名;专职高级职称5名,中级职称5名;博士5名,本科5名。
全体临床试验相关人员均已完成国家药品监督管理局(NMPA)要求的药物临床试验质量管理规范(GCP)培训;
部分人员通过了美国临床研究专业协会(ACRP)组织的ICH-GCP考试;部分人员参加哈佛医学院全球临床研究培训 (GCSRT)并通过考核。
三、组织结构图
同济医院I期临床试验研究室隶属于华中科技大学同济医学院附属同济医院国家药品临床试验机构,分为临床部和质量部。
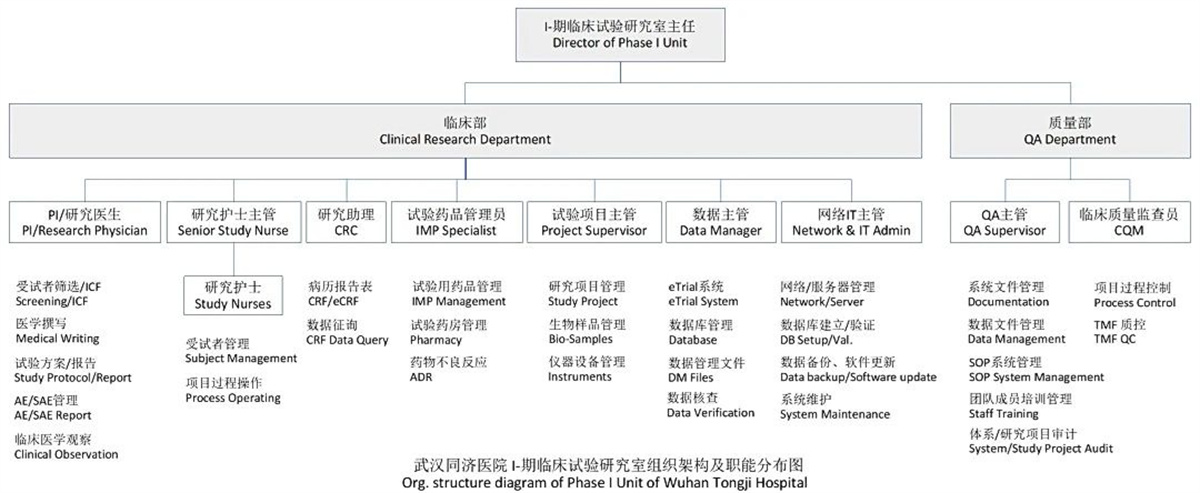
四、I期临床质量管理体系
本中心按高标准进行质量体系建设:已完成正式项目的全流程电子化操作,中英文双语质量体系已通过Pharmazone认证,具备承接创新药I期临床试验及生物等效性(BE)研究的资质。
五、成果及特色项目
本中心是国内最早一批获得药物临床试验资格的临床试验机构之一,已完成项目百余项,包括耐受性试验(含注射剂和口服剂)、药代动力学试验、生物等效性试验和一致性评价。722之后,已承接项目80余项,本中心722之后已通过国家局核查(含免核查)的项目近30余项。
研究室自成立至今已完成项目百余项,包括:
人体耐受性试验、药代动力学试验(PK)、生物等效性试验(BE)、药物相互作用试验(DDI)、PK/PD 试验
涉及药物种类:
抗肿瘤药物、精神类药物、呼吸系统药物、生物制剂、靶向制剂……
涉及药物剂型:
注射剂、栓剂、 滴鼻剂、片剂、胶囊剂……
作为子课题参与国家重大新药创制课题两项,包括:
1)“十二五”课题:泌尿生殖系统肿瘤的国际化新药临床研究技术平台建设;
2)“十三五”课题:具有先进技术特色的糖尿病新药临床评价综合服务创新平台体系建设。

六、联系方式
I期临床试验研究室办公室主任:
李娟,027-83662379,tongjigcp2@163.com
I期临床试验研究室项目主管:
任秀华,027-69378207,xiuhua.r@tjh.tjmu.edu.cn
七、研究室地址
湖北省武汉市蔡甸区新天大道288号同济医院中法新城院区门诊C区5楼
同济医院I期临床试验研究室介绍
